어느새 시총 3조에 육박한 에이비엘바이오에 대해서
공부를 해보려고 한다.
IR자료가 굉장히 두껍지만..
회사에서 5월에 업로드한 자료를 하나하나 보려고 한다.
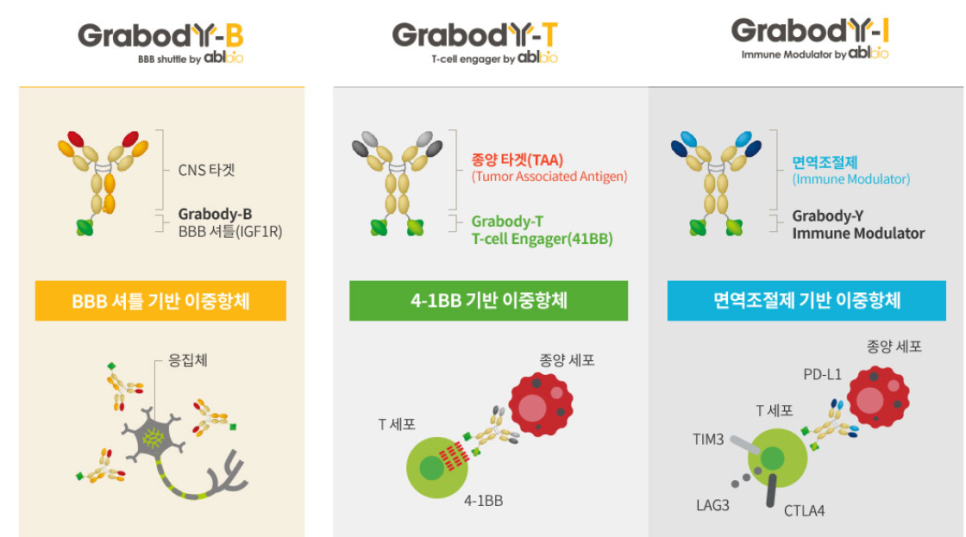
그랩바디 파이프라인은 잘 체크!
Grabody-B: 뇌혈관장벽(BBB)을 통과하는 이중항체 - 뇌질환 치료용
Grabody-T: T세포 자극(4-1BB)을 이용해 암세포를 공격 - 항암 치료용
Grabody-Y: 면역억제 신호 차단으로 면역 활성화 - 면역항암제
본문 핵심만 요약하면

ABL바이오는 BBB 셔틀(Grabody-B), T세포 자극 플랫폼(Grabody-T), 이중항체 기반 ADC 등 독자적 기술력을 바탕으로 글로벌 빅파마와의 기술이전과 임상 확장을 이어가고 있음.
ABL001(담도암 치료제)은 FDA 패스트트랙 지정을 받아 상용화 가능성이 높고, Grabody-B는 GSK 등과의 대형 계약으로 플랫폼 가치가 입증됨.
이중항체 ADC 파이프라인도 미국 현지 개발 체계를 구축하며 IND 진입을 앞두고 있어 성장 기대가 큼.
임상 성과·기술이전 모멘텀에 따라 기업가치 재평가 가능성이 있으나, 경쟁 심화 및 임상 변수에 따른 리스크도 상존함.
회사만의 경쟁력은
대체불가능한 경쟁력은..
이중항체 기반 4세대 ADC 개발 역량: Grabody-T 플랫폼을 기반으로 면역세포 활성화와 타겟 선택성을 동시에 확보, 타사 대비 독보적인 이중항체 ADC 기술력을 확보 .
뇌혈관장벽(BBB) 셔틀 기술 Grabody-B: 기존 단일항체가 뚫지 못한 뇌질환 치료에 강력한 해결책을 제시하며, 글로벌 제약사들과의 협업 및 기술이전의 발판이 됨 .
검증된 임상 결과와 FDA Fast Track 지정: ABL001, ABL111 등 주요 파이프라인에서 미국 FDA의 패스트트랙 지정을 받으며 상업화 기대감 상승 .
전략적 타겟 조합과 시너지 극대화: CLDN18.2, B7-H4, ROR1, 4-1BB 등 글로벌 톱티어 타겟들과의 조합으로 차세대 면역항암제 개발을 선도 .
글로벌 시장을 겨냥한 선제적 포트폴리오 구성: 미국, 유럽, 아시아 4개국에 걸친 임상 진행 및 다수의 라이선스 아웃 계약으로 상업화 가능성과 확장성 모두 확보 .
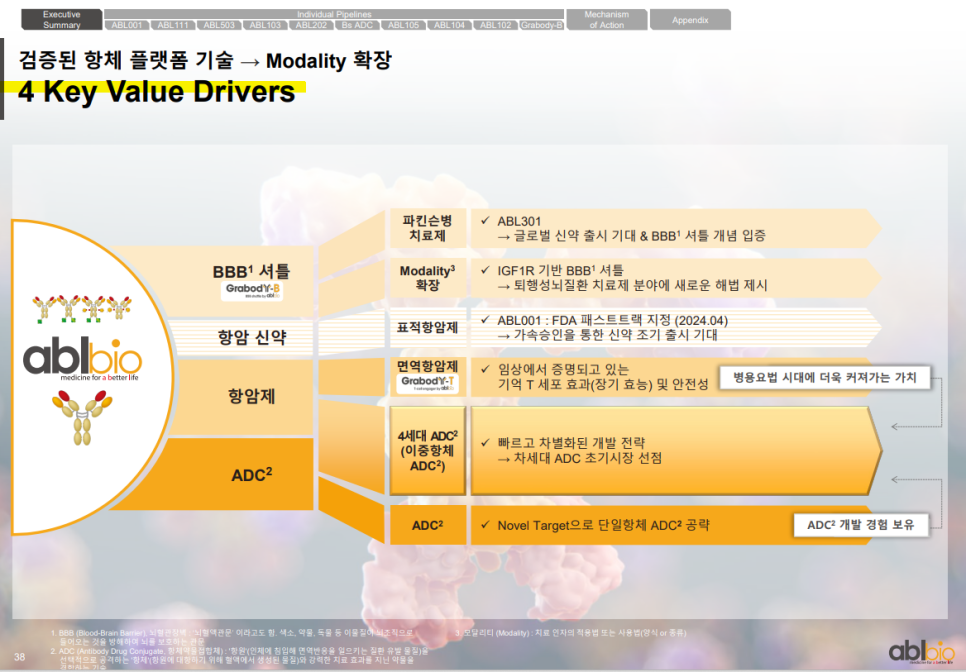
ABL바이오는 BBB 셔틀, 면역항암제, ADC 등 검증된 항체 플랫폼 기술을 기반으로 다양한 모달리티로 확장 중에 있음.
Grabody-B 플랫폼은 IGF1R 기반 BBB 셔틀로 퇴행성 뇌질환에 대한 새로운 해법을 제시하고 있음.
Grabody-T 플랫폼은 기억 T세포 활성화를 통한 장기 효능과 안전성이 임상에서 입증되고 있음.
이중항체 기반 ADC(4세대)는 빠르고 차별화된 전략으로 글로벌 선도 기술 확보에 집중하고 있음.
항암 신약 ABL001은 FDA Fast Track 지정을 바탕으로 빠른 상용화가 기대되고 있음.
ABL바이오는 Grabody-B/T, ADC 등
핵심 기술 플랫폼을 모두 보유한 ‘풀스택 항체 기업’으로 평가될 수 있다.
이것 자체만으로도 경쟁력이 아닐까..
단일 파이프라인 의존이 아닌 다중 모달리티 전략은
중장기적 글로벌 경쟁력과 기업가치 상승의 기반이 된다
.특히 BBB 셔틀과 ADC는 경쟁사 대비 빠른 임상 진입과 독자적 기술
내재화로 ‘First & Best-in-Class’ 포지션을 추구하고 있다.

ABL바이오는 검증된 항암 타깃(CLND18.2, PD-L1, HER2 등)을 중심으로 개발 리스크를 낮추고 있고
기술이전 이력이 풍부하며, AstraZeneca·GSK·Merck 등
글로벌 빅파마와의 계약 실적은 신뢰도를 높인다.
ROR1·a-syn 등 고난도 질환에 대한 선제적 접근은 장기 성장성과 파이프라인 확장성을 시사하며
플랫폼 기술력과 타깃 전략의 조화는 기술이전, 공동개발, 상용화 등
다방면 수익 모델로 이어질 수 있음.

ABL바이오는 Grabody 플랫폼 기반으로 각 타깃(CLND18.2, 4-1BB, IGF1R 등)과의
조합을 통해 경쟁약물 대비 효능·안전성 모두를 강화하고 있다.
특히 BBB 셔틀과 4-1BB 이중항체는 기존 한계를 극복하며
빠른 임상 진입과 글로벌 기술이전 성과로 이어지고 있다.
다양한 타깃 기반 이중항체 ADC는 향후 블록버스터 잠재력을 가진 파이프라인으로 주목받고 있음.
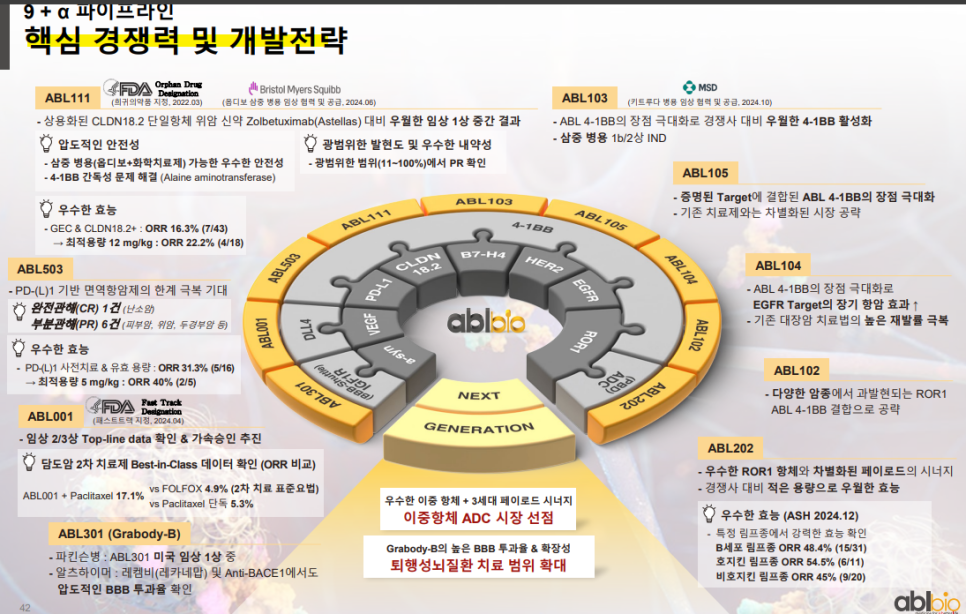
ABL바이오는 CLDN18.2·4-1BB·ROR1 등 다양한
검증된 타깃 기반의 이중항체 ADC 포트폴리오를 확보하고 있으며,
주요 파이프라인은 글로벌 빅파마와 공동개발 또는 기술이전 중이다.
각 파이프라인은 기존 치료제 대비 우월한 ORR, 낮은 독성, 폭
넓은 적응증을 기반으로 임상 성과를 도출 중이며 일부는 이미 FDA Fast Track 지정.
특히 Grabody-B 플랫폼을 통한 BBB 셔틀 기술은
퇴행성 뇌질환까지 적응증을 확장시킬 수 있어 장기적으로도 성장성이 높다.
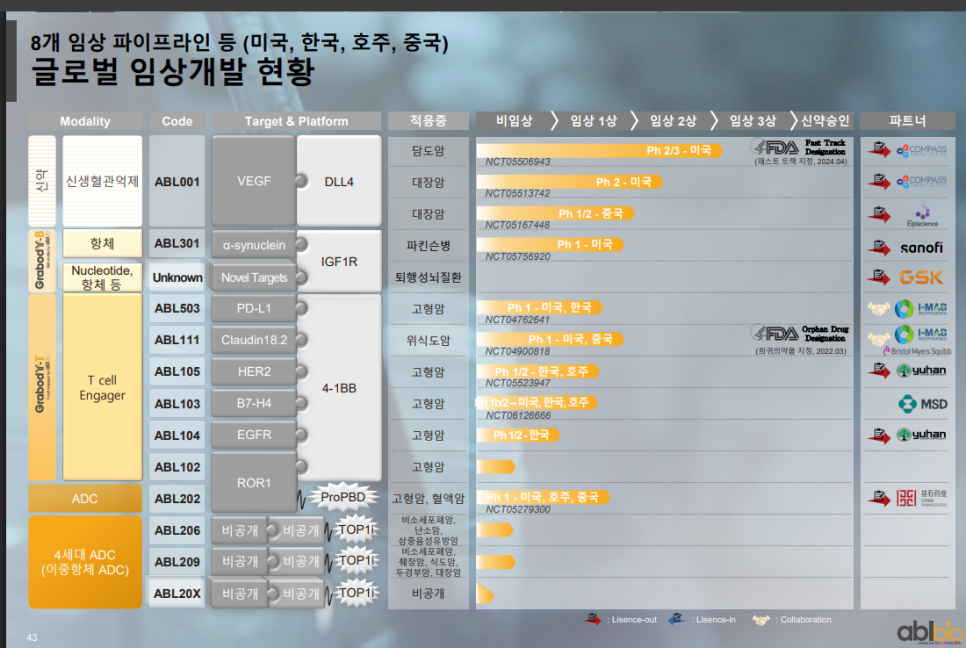
ABL바이오는 미국, 중국, 한국, 호주 등에서
8개 파이프라인을 통해 글로벌 임상을 활발히 진행 중이며,
일부는 FDA Fast Track 및 희귀의약품 지정까지 받았다는 부분을 주목할 수 있음.
Grabody-B와 Grabody-T 플랫폼 기반의 파이프라인은 다양한 암종 및 퇴행성 뇌질환까지 확장성 확보.
특히 ABL001(대장암)과 ABL301(파킨슨병)은 글로벌 빅파마와 협력하여 임상 2/3상, 1상 진입 중.
이중항체 기반 4세대 ADC도 본격 개발되며 중장기 성장 동력으로 작용 가능.
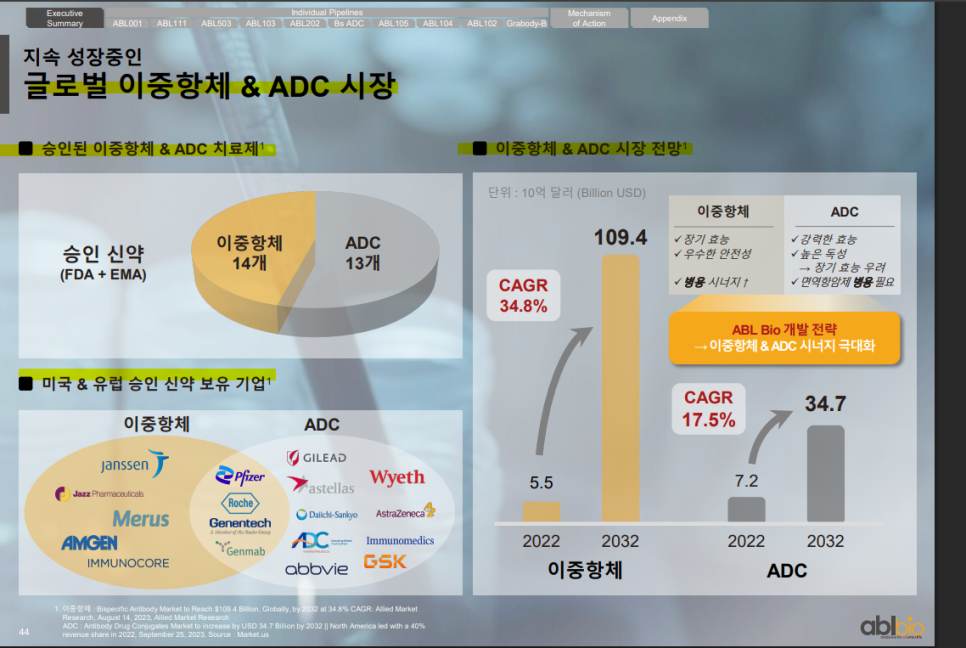
이중항체와 ADC 시장은 각각 연평균 34.8%, 17.5%로 고성장 중이며,
2032년까지 총 시장 규모가 140조 원 이상으로 확대 전망되고 있음.
ABL바이오는 두 플랫폼의 시너지를 활용한 전략으로 빠르게 성장하는 글로벌 흐름에 정면 대응 중임.
FDA/EMA 승인 신약을 보유한 글로벌 빅파마들이 이미 시장 선점 중이며,
ABL바이오의 차세대 ADC 경쟁력은 이들과의 파트너링 가능성도 시사중이다.
IR자료를 보면
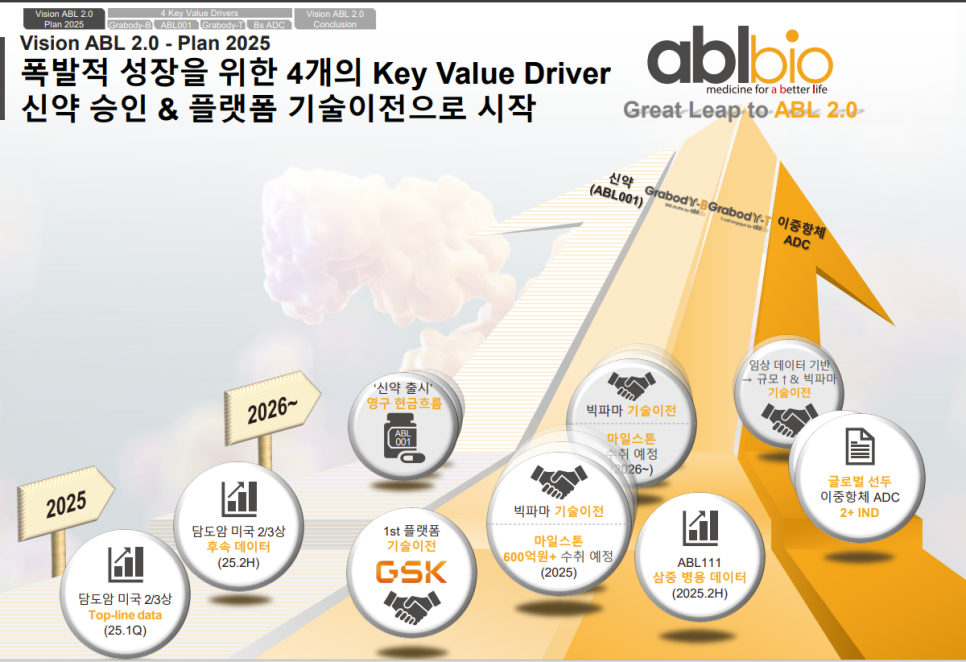
ABL Bio는 2025년까지 4대 핵심 가치동인을 중심으로 성장 전략을 추진 중에 있음.
ABL001 신약 출시, Grabody-B 기반 플랫폼 기술이전, 이중항체 ADC 개발이 주요 축으로 작용하고 있음.
담도암 임상 2/3상 데이터, GSK 및 빅파마와의 기술이전, 글로벌 IND 진입 등의 마일스톤이 예정되어 있음.
2025년 주요 임상 결과와 기술이전 수익(600억+)은 기업 가치 상승의 촉매제가 될 수 있고.
ABL001의 출시 및 상용화는 첫 번째 신약 수익화라는 큰 전환점을 의미함.
이중항체 ADC 및 Grabody-B 플랫폼은 글로벌 제약사 대상 추가 기술이전 가능성을 높임.
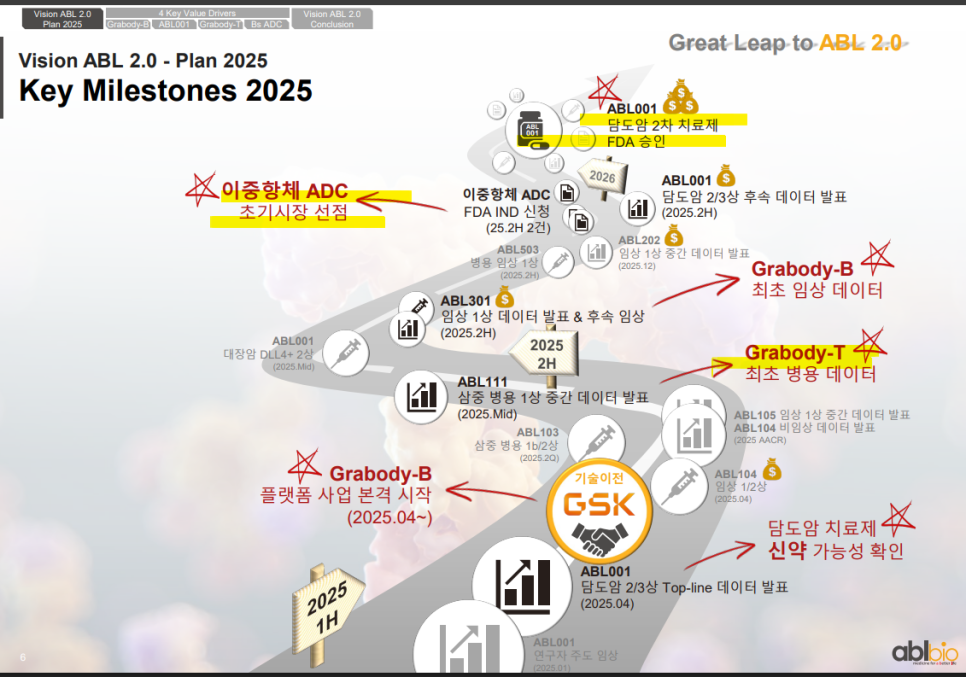
2025년은 Grabody-B/T의 첫 임상 및 병용 데이터 확보와 플랫폼 사업 본격화가 예정되어 있음.
ABL001은 담도암 치료제로서 Top-line 결과 발표와 FDA 승인 목표가 설정되어 있음.
이중항체 ADC는 IND 신청 및 초기 시장 선점을 위한 진입 단계에 있음.
2025년은 ABL001의 FDA 승인 가능성과 매출 본격화 여부를 확인할 핵심 시점임.
Grabody-B/T 플랫폼 임상 성과는 기술이전 및 파이프라인 확장의 지렛대 역할을 할 수 있음.
이중항체 ADC의 전임상 진전은 차세대 성장동력으로 주목 가능함.
그랩바디B

Grabody-B는 IGF1R 기반의 차세대 BBB 셔틀 플랫폼으로, 기존 단일항체의 한계를 극복할 기술로 주목받고 있음.
경쟁사들은 TfR 기반 셔틀 확보에 집중 중이나, Grabody-B는 글로벌 임상 1상 데이터를 축적하며 가장 빠르게 입증되고 있음.
기존 승인 신약들(아두헬름, 레켐비 등)은 안전성 한계(ARIA-E 등)로 한계가 존재하고 있음.
Grabody-B는 경쟁이 치열한 BBB 셔틀 시장에서 임상 데이터 기반의 차별화된 선두 입지를 확보 중이고
기존 제품 대비 안전성과 효능 모두에서 우위 가능성을 내포하고 있다.
글로벌 제약사들의 M&A 및 파트너십 움직임은 Grabody-B의 가치 재평가 가능성을 높이고 있다.

Grabody-B는 IGF1R 기반 BBB 셔틀 최초 플랫폼으로, GSK와의 기술이전을 통해 본격적인 사업화가 진행 중에 있음.
총 계약 규모는 4.1조원에 달하며, 이 중 계약금 및 단기 마일스톤으로 1,480억 원이 확보되어 있음.
글로벌 제약사들의 CNS/ADC 플랫폼 기술 확보 경쟁이 심화되는 가운데, Grabody-B는 빠른 IGF1R 셔틀 선점으로 주목받고 있음.

Grabody-B는 단일기술로 1조 원대 계약도 가능한 글로벌 플랫폼으로 부상하고 있다는 부분은
정말 주목을 할만한 부분임.
GSK와의 첫 기술이전은 후속 대형 딜 유치 및 기업가치 재평가의 전환점이 될 수 있고
CNS·ADC 시장 내 선도적 입지를 바탕으로 파이프라인 확장과 수익 다각화가 기대된다.
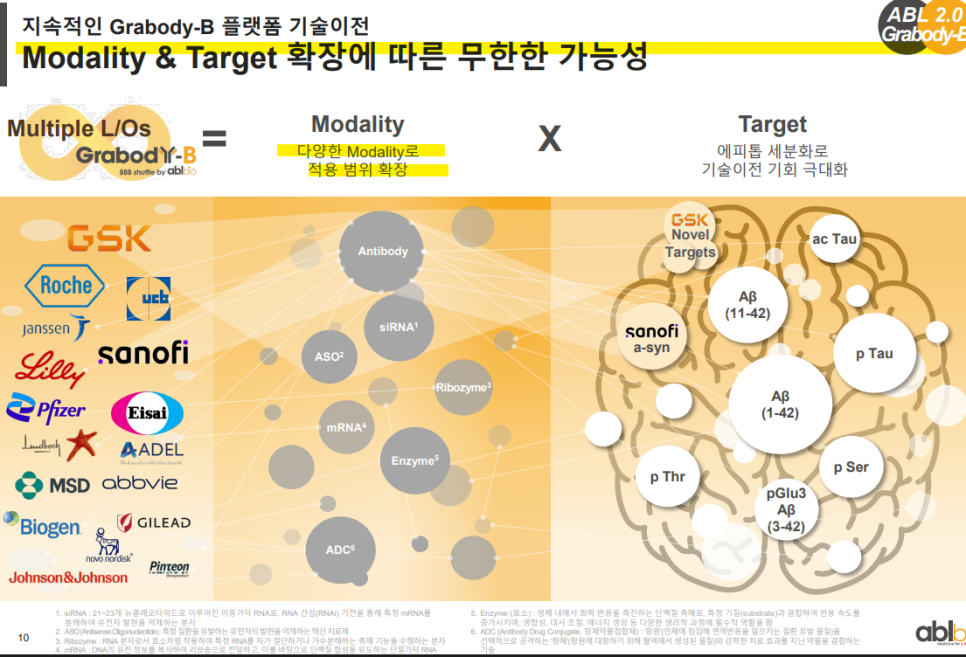
Grabody-B는 다양한 modality (항체, siRNA, mRNA 등)와 target (Aβ, Tau, α-syn 등)에 적용 가능한 확장성이 입증되고 있음.
글로벌 제약사(GSK, Sanofi, Pfizer 등)와의 협업을 통해 modality 및 target 다변화 기회를 적극 확보하고 있음.
기술이전 기회는 특정 적응증을 넘어서 에피톱 세분화 및 치료 전략 다양화로 확대되고 있음.
Grabody-B는 단일 플랫폼이 아닌 다중 modality와 결합 가능한 범용 기술로, 확장성과 지속성이 크며
파트너사 스펙트럼이 폭넓고, 각각의 타깃에 따라 기술이전 수요도 계속 증가 가능성이 있다,
향후 기술이전 건 수와 계약 규모 모두 기하급수적 성장 가능성을 내포하고 있음.
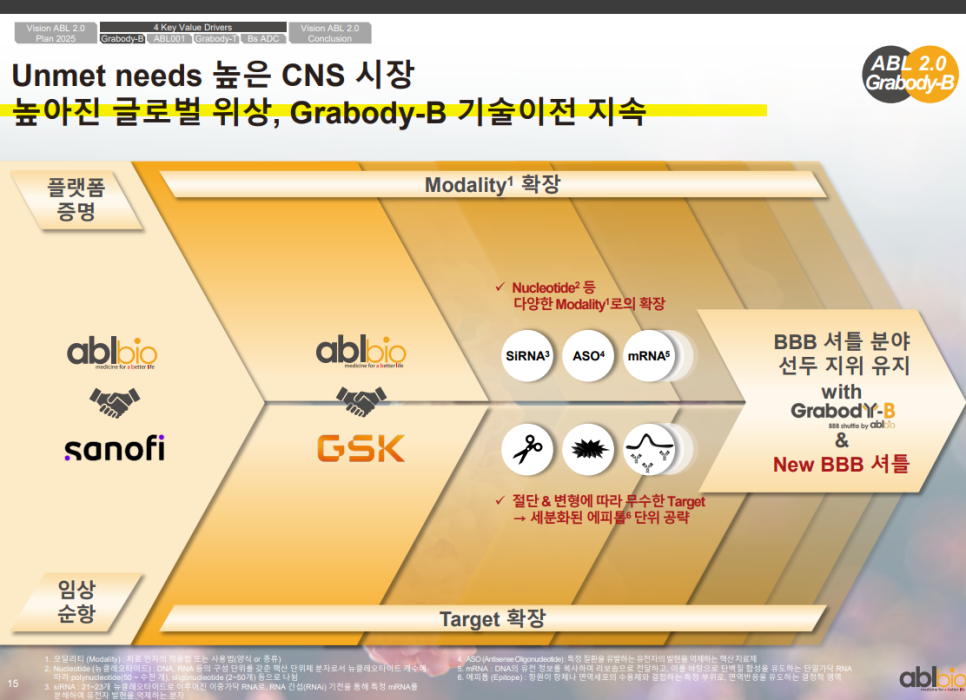
Grabody-B는 Sanofi, GSK와의 협업을 통해 플랫폼 기술력을 임상 단계에서 입증하고 있음.
다양한 Nucleotide 계열(Modality)로 확장 가능성이 열려 있으며, siRNA, ASO, mRNA 등에도 적용이 가능함.
질환 유형과 변형에 따른 다양한 타겟을 공략함으로써 세분화된 CNS 시장 내 입지를 넓히고 있음.
계속 나오는 이야기지만
Grabody-B는 단일 질환에 국한되지 않고 다양한 modality와 target으로 확장 가능성이 큼.
글로벌 제약사와의 협업을 통해 임상 및 상업화 타당성을 이미 검증 중임.
CNS 분야에서 기술 리더십을 유지하며 New BBB 셔틀 개발로 후속 파이프라인 기대감도 높다.
ABL001

담도암 치료제인 ABL001이다.
담도암은 간에서 만들어진 담즙이 흐르는 통로인 담도에 생기는 암이고
주요 증상으로는 황달, 복통, 가려움증 등이 있으며 조기 발견이 어렵다.
치료는 수술, 항암치료, 방사선 치료 등이 있으며 진행 단계에 따라 다르다.
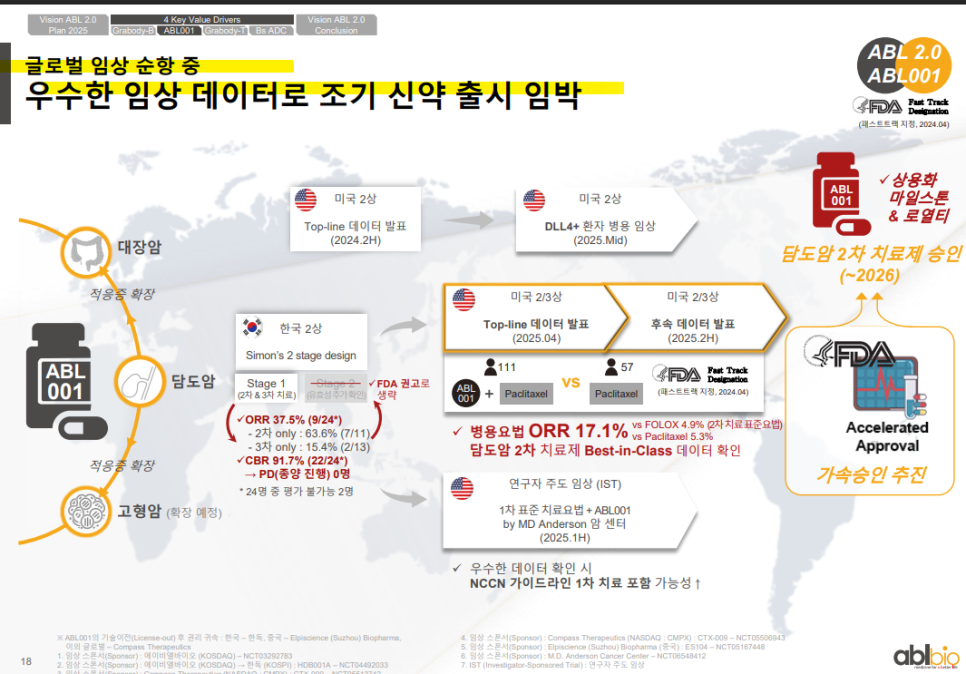
ABL001은 담도암 2차 치료제로서 미국 2/3상 임상에서 Best-in-Class 수준의 유효성이 입증되고 있음.
2025년 상반기 Top-line 데이터 발표 이후 하반기에는 후속 데이터 공개 및 FDA Accelerated Approval 추진이 예정되어 있음.
한국 임상 결과에서도 높은 반응률(ORR 37.5%, CBR 91.7%)을 보여 FDA 권고로 3차 환자 모집 없이 2상 완료됨.

ABL001은 담도암 2차 치료제로서 FDA 가속승인과 상용화 가능성이 매우 높고
미국·한국 임상에서 경쟁 치료 대비 뛰어난 결과가 확인되어 블록버스터 신약 가능성이 있음.
상용화 시점(~2026년)까지 다수의 마일스톤 및 로열티 수익 창출 기대감이 큼.
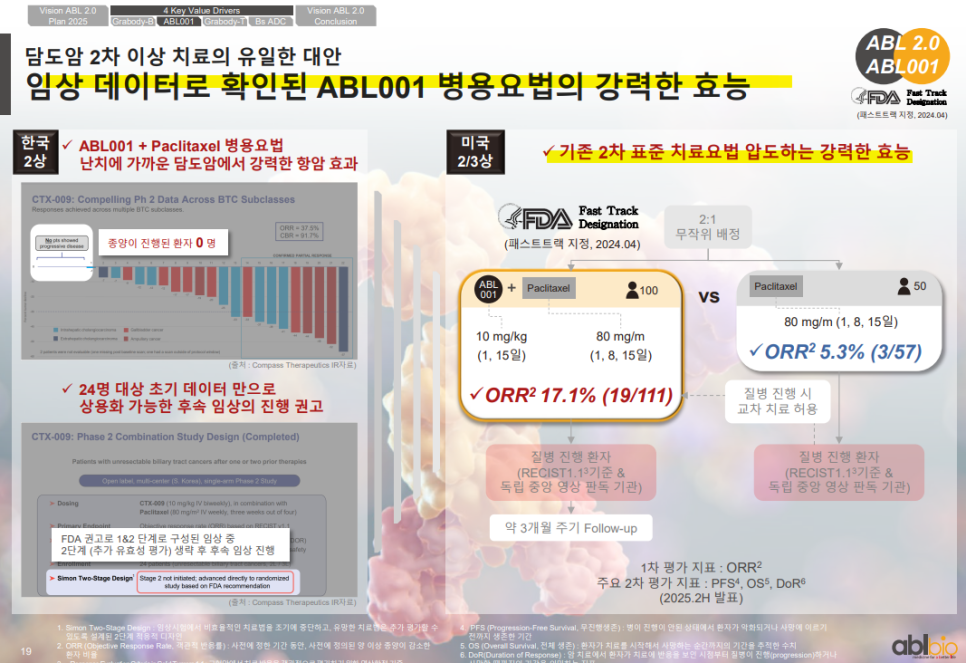
ABL001 병용요법은 기존 2차 치료법(Paclitaxel 단독) 대비 ORR 3배 이상의 효과(17.1% vs 5.3%)를 입증하고 있음.
한국 임상 2상에서도 ORR 37.5%, CBR 91.7% 등 탁월한 항암 효과가 확인되어 FDA로부터 후속 임상 권고를 받은 바 있음.
질병 진행 억제, 중앙 영상 판독 기준 통과 등에서 높은 신뢰성을 확보하고 있음.
ABL001은 병용요법으로서 기존 치료제 대비 탁월한 효능을 확보, 대체 치료제로서 경쟁력이 높고
Fast Track 지정 및 FDA 권고 기반으로 상용화 가능성이 빠르게 현실화될 가능성 있다.
긍정적인 임상지표는 기술이전 및 글로벌 확장 전략에도 유리하게 작용할 수 있음.
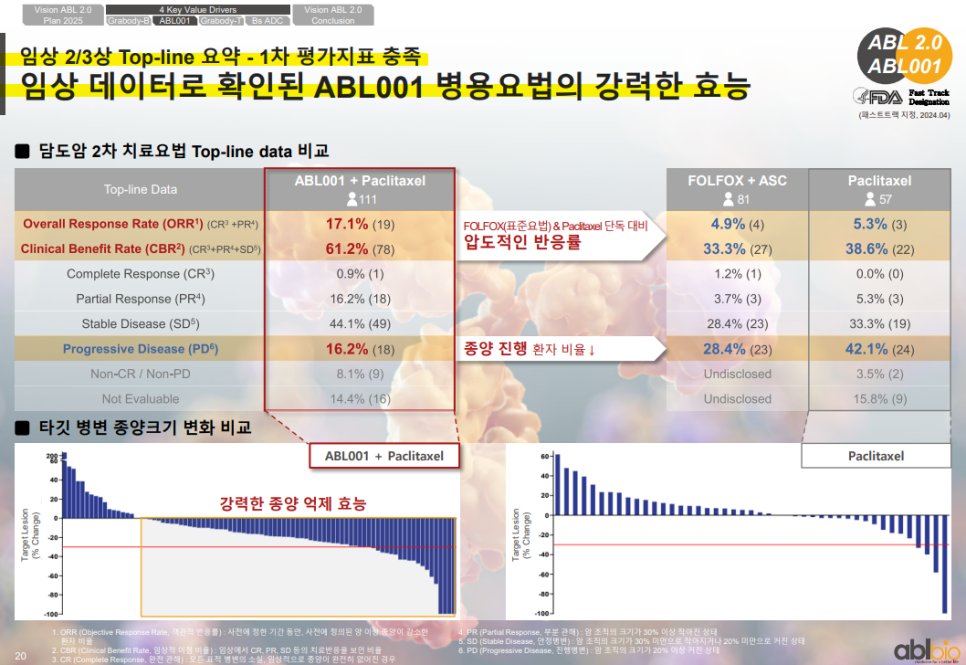
ABL001 병용요법(ABL001 + Paclitaxel)은 ORR 17.1%, CBR 61.2%로 기존 치료 대비 압도적인 반응률을 기록하고 있음.
표준요법(FOLFOX+ASC, Paclitaxel 단독)의 ORR은 각각 4.9%, 5.3%에 불과해 상대적 우월성이 입증되고 있음.
타깃 병변 억제 효과에서도 ABL001 병용군이 강력한 중앙 크기 감소 효과를 보여주고 있음.
ABL001 병용요법은 기존 대비 3배 이상의 반응률로 FDA 승인 가능성을 높이고 있다.
경쟁 치료 대비 월등한 효능은 상용화뿐 아니라 글로벌 기술이전에도 유리하게 작용함.
종양 억제력 시각화 데이터는 투자자 신뢰도와 파트너 유치에 핵심 증거로 활용될 수 있음.

ABL001은 미국 2/3상 임상에서 ORR 17.1%를 기록하며 기존 2차 표준 치료요법(FOLFOX, Paclitaxel)을 압도하고 있음.
1차 치료제 후보로도 개발 중이며, 기존 면역항암제 대비 효능·안전성에서 우위를 확보할 가능성이 있음.
2025년 하반기 발표 예정인 생존 지표(mOS, mPFS 등) 결과가 임상적 전환점이 될 것으로 기대되고 있음.
ABL001은 2차 치료제에서 입증된 성과를 기반으로 1차 치료제로의 확장 가능성이 높고
글로벌 임상 진입과 FDA Fast Track 지정은 상용화·기술이전 기회의 가시성을 높임.
향후 생존 지표 발표는 신약 가치 재평가의 중요한 계기가 될 수 있다..
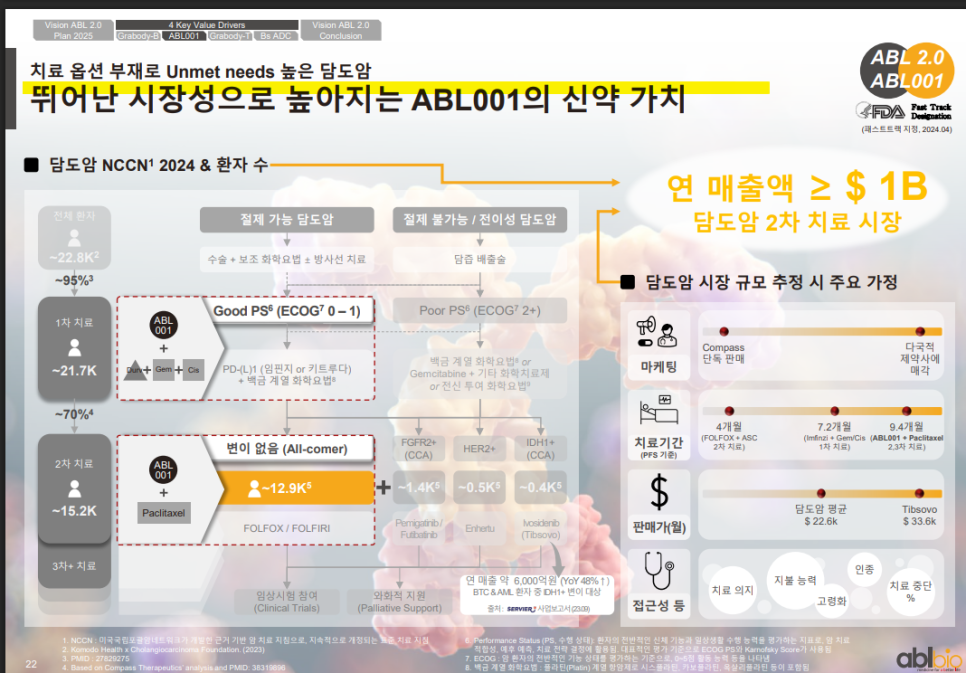
ABL001은 담도암 2차 치료제로 약 1.3만 명의 환자군을 대상으로 시장 진입이 가능할 것으로 추정되고 있음.
담도암 전체 환자 중 약 70%가 2차 치료에 진입하며, ABL001은 이들 중 대부분을 커버할 수 있는 범용 치료제 역할을 하고 있음.
시장 규모와 적정 약가를 기반으로 연 매출 $1B 이상 달성 가능한 신약 가치를 보유하고 있음.
담도암 2차 치료 시장은 고정 수요와 제한적 경쟁 덕분에 고성장이 가능한 틈새 블록버스터 영역이며
ABL001은 넓은 적응증 범위와 병용 요법 강점을 바탕으로 시장 점유율 확보 가능성이 높다.
Compass 대비 더 긴 치료기간과 다국적 제약사로의 이전 가능성은 매출 극대화에 유리한 구조임.
그랩바디-T
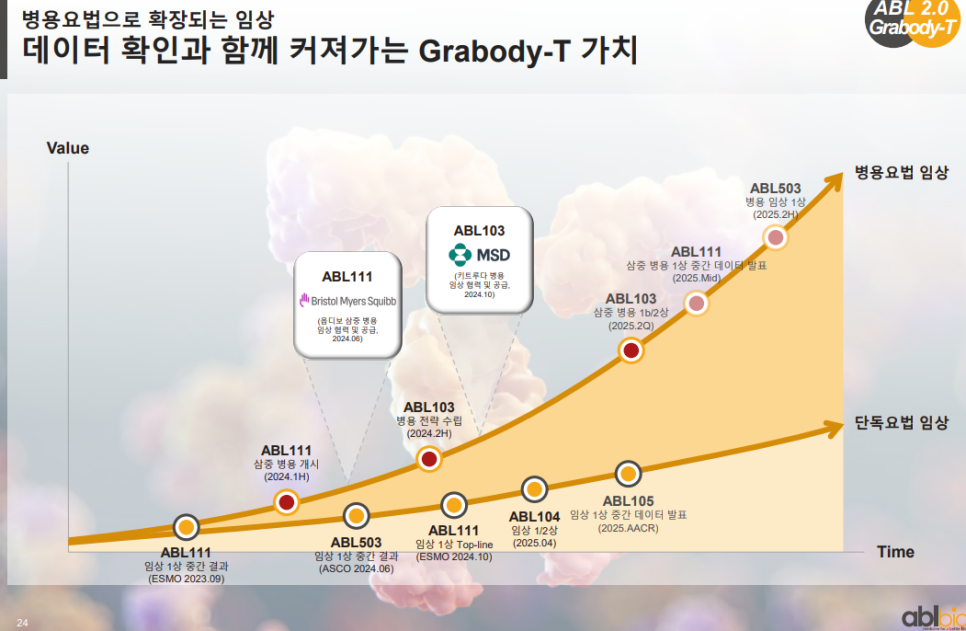
Grabody-T는 병용요법 중심으로 임상이 확장되며 데이터 축적에 따라 가치가 빠르게 상승하고 있음.
ABL111·103·503 등의 병용 임상이 진행 중이며, 브리스톨 마이어스 스퀴브(BMS)와 MSD 등 글로벌 빅파마와 협력 중에 있음.
2025년까지 다수의 중간/Top-line 데이터 발표가 예정되어 있어 임상 진전 속도가 빠르게 가속되고 있음.
Grabody-T 플랫폼은 단독요법을 넘어 병용 임상으로 확장되며 기술이전 기대치를 높이고 있고
글로벌 제약사들과의 협업은 후속 파이프라인의 신뢰성과 상용화 가능성을 높여주는 근거가 있음.
2024~2025년 집중되는 임상 성과 발표는 플랫폼 전체의 기업가치 재평가 촉매가 될 수 있음.

Grabody-T는 4-1BB 이중항체 플랫폼으로, 비임상에서 장기 효능 및 우수한 안전성을 확인한 후 임상에서 그 잠재력을 입증 중에 있음.
ABL111은 삼중 병용요법 임상에서 중간 결과 발표(2025.2H)를 앞두고 있으며, Bristol Myers Squibb와의 협업을 통해 플랫폼 가치가 입증되고 있음.
ABL103은 MSD와 함께 키트루다 병용 임상(1b/2상) 진입 예정으로, 기술이전 가능성도 가시화되고 있음.
Grabody-T 플랫폼은 면역자극과 T세포 형성의 균형을 통해 차별화된 병용 요법 효능을 확보하고 있고
글로벌 빅파마와의 공동 개발은 신뢰성과 상용화 가능성을 높이는 핵심 지표이다.
다수의 병용 임상 진입과 데이터 확보는 기술이전 및 플랫폼 가치 상승으로 직결될 수 있음.

ABL111은 CLDN18.2 발현율 11~100%의 광범위한 환자군에서 안전성과 효능이 입증되고 있음.
경쟁 약물인 Zolbetuximab은 고발현(≥75%) 환자에만 효과를 보이는 단일항체로, 한계가 존재하고 있음.
ABL111은 저발현(27.6%) 환자군까지 커버 가능한 이중항체로, 시장 확장성과 차세대 Best-in-Class 가능성을 보유하고 있음.
ABL111은 단일항체 대비 넓은 타깃 커버리지로
위암 치료제 시장에서 차별화된 경쟁력을 확보하고 있고
발현율이 낮은 환자군까지 포함 가능하다는 점은 시장 저변 확대 및 매출 성장의 핵심 근거가 된다.
경쟁 약물 대비 후발주자이지만, 더 폭넓은 적응증으로 글로벌 기술이전 및 블록버스터 가능성이 기대된다.
일본 VYLOY(졸베툭시맙) 실적 기준 연매출 1조 원 이상 시장도 충분히 겨냥할 수 있음.

ABL111은 단독요법 및 삼중 병용요법 모두에서 Zolbetuximab 대비 효능과 안전성 면에서 경쟁우위를 입증하고 있음.
CLDN18.2 발현률이 낮은 환자군(≥21%)에서도 의미 있는 ORR과 CBR을 보여 더 넓은 환자 풀에서 사용 가능성이 있음.
ABL111은 간독성, 위장장애 등 주요 부작용에서도 낮은 발생률을 보여 우수한 내약성을 확보하고 있음.
삼중 병용요법 중간 데이터는 2025년 중 발표 예정으로, 플랫폼 가치 상승의 촉매 역할을 할 것으로 기대됨.

ABL111은 단일항체 대비 낮은 독성과 높은 반응률로 차세대 CLDN18.2 치료제로서의 입지를 굳히고 있음.
고발현 환자뿐 아니라 저발현 환자까지
커버 가능한 이중항체로, 시장 점유율 확대 가능성이 큼.
특히 삼중 병용요법은 Zolbetuximab보다 뛰어난 효과를 예고하며,
글로벌 제약사 기술이전 및 병용 전략의 핵심 자산으로 주목됨.
향후 임상 중간 결과 발표 시점이 기업가치 재평가의 주요 변곡점이 될 수 있음.

ABL503은 단독요법에서 ORR 31.3%, CBR 75.0%를 기록하며 PD-L1 사전 치료 환자 대상 강력한 항암 효과와 안전성이 확인되고 있음.
경쟁 후보인 Genmab의 GEN1046 대비 높은 반응률과 낮은 간독성을 보이며, 간 손상 지표(Bilirubin 상승 등)도 나타나지 않았음.
7회 이상 치료에 실패한 난소암 환자에게도 4개월 이상 지속적인 종양 억제 효과가 확인되며, 기억 T세포 형성을 통한 장기 효과도 입증되고 있음.
ABL503은 경쟁 이중항체 대비 월등한 ORR/CBR과
낮은 독성 프로파일로 Best-in-Class 가능성을 보여주고 있고
기존 치료에 실패한 고난도 환자 대상 완전 관해 사례는
임상적 희소성과 확장성 측면에서 매우 주목할 만함.
유도 효과는 병용뿐 아니라 단독요법의 장기 효능 확보에도
강력한 근거가 되며, 기술이전 가치도 상승시킬 요소임.
Grabody-T는 경쟁 약물이 직면한 간독성 한계를 극복하며
안전성과 효능 두 마리 토끼를 잡은 플랫폼이다.
병용 임상 확대는 단일 제품이 아닌 플랫폼으로서의 상업적 잠재력을 강화하는 요인이 됨.
ABL111 임상 결과에 따라 다수의 병용 파이프라인의 가치도 함께 상승할 가능성이 높음.
지속적인 데이터 축적은 기술이전 및 글로벌 파트너십 확대의 기반이 될 수 있음.
에이비엘바이오의
ADC까지
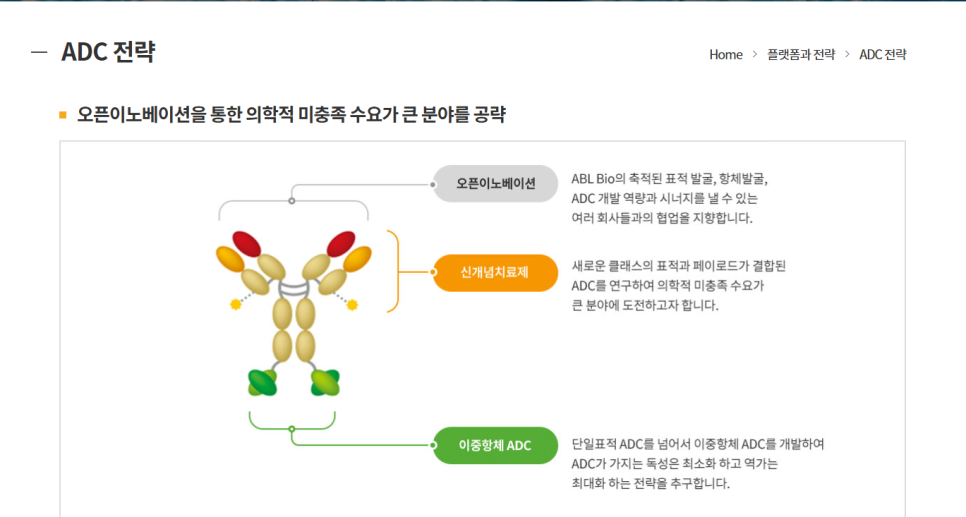

ABL Bio는 이중항체 ADC 시장 선점을 위해 미국 현지 법인(ABL Bio USA)을 중심으로 전략을 실행하고 있음.
글로벌 제약사 출신 인력을 영입하여 ADC 기술 내재화에 성공하고 있음.
ABL206, ABL209 등의 검증된 항체를 기반으로 Synaffix 등 외부 플랫폼을 결합한 TOP1i 기반 ADC 기술도 확보하고 있음.
1,400억 원 규모의 자금을 바탕으로 개발 속도 단축 및 시장 가치 극대화를 추진하고 있음.
ADC 전문 인력과 기술 내재화를 바탕으로
글로벌 이중항체 ADC 시장에서 First-in-Class를 노릴 수 있는 입지에 있다.

미국 법인을 거점으로 한 R&D 집중은 기술이전뿐 아니라
직접 개발을 통한 밸류 체인의 확장 가능성을 보여준다.
대규모 자금 확보와 검증된 파이프라인은 조기 임상 진입과
기술 상업화 속도를 높일 핵심 기반이다.
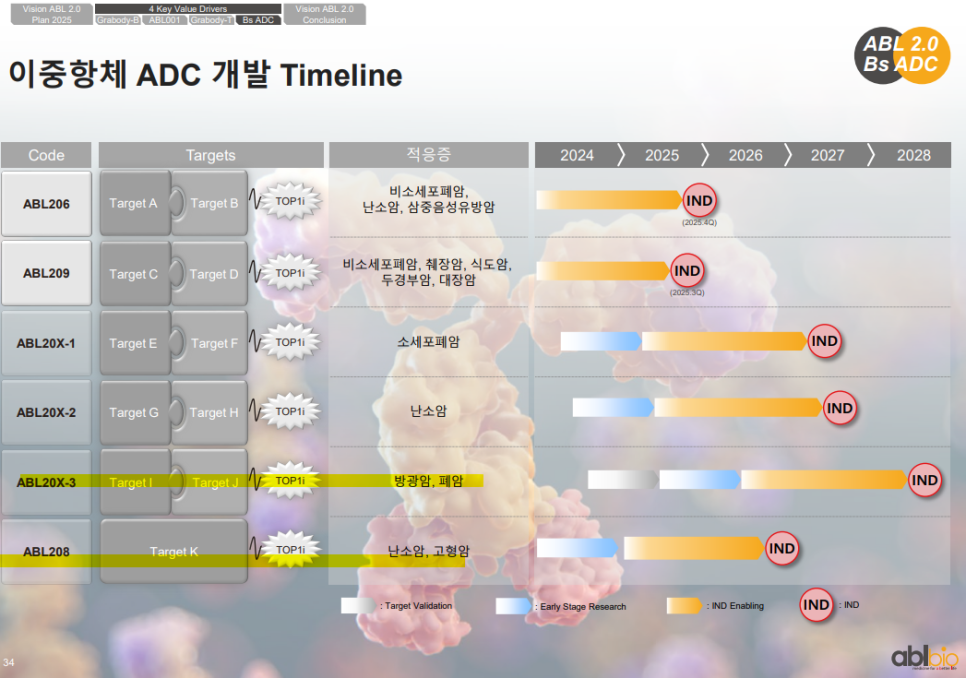
ABL Bio는 총 6개의 이중항체 ADC 파이프라인을 보유하고 있으며 모두 TOP1i 기반 플랫폼 기술을 적용하고 있음.
ABL206과 ABL209는 각각 2025년 3분기와 4분기 중 IND(임상시험계획) 신청이 예정되어 있음.
나머지 파이프라인(Abl20X 계열, ABL208)은 다양한 고형암(소세포폐암, 난소암, 방광암 등)을 타깃으로 2026~2028년 IND 진입을 목표로 하고 있음.
전체 파이프라인이 타깃 검증 → 초기연구 → IND Enabling 단계를 거치며 순차적으로 개발되고 있음.
2025년 ABL206/209의 IND 진입은 ABL Bio 이중항
체 ADC 기술의 상업화 가능성을 현실화하는 첫 시점이다.
다양한 암종을 겨냥한 파이프라인 다변화는 리스크 분산과 장기적 성장 모멘텀 확보에 기여하며
모두 TOP1i 기반의 독자적 플랫폼을 적용하고 있어, First-in-Class 및 기술이전 기대감이 높다.
연속적 IND 진입 로드맵은 장기 투자 관점에서 밸류에이션의 지속적 레벨업 가능성을 시사한다.
앞으로의 주가 전망은
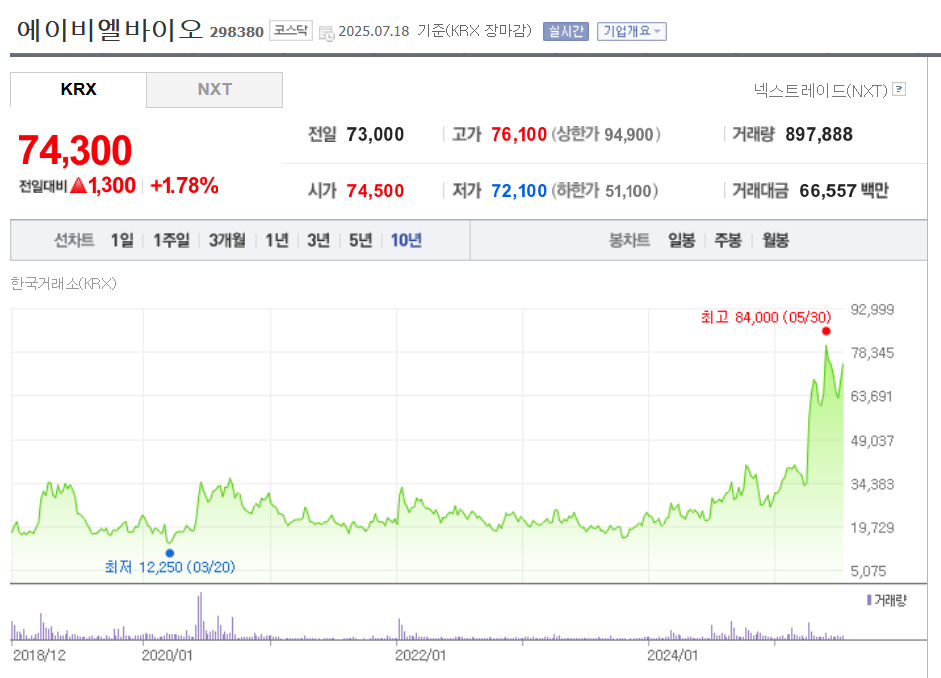
1.긍정적 전망
FDA 패스트트랙 지정, 빅파마와의 연속적 기술이전, 이중항체 ADC 및 BBB 셔틀 기술 등 독보적 플랫폼 기반으로 글로벌 가치 재평가 가능성이 큼.
2025~2026년 주요 임상 결과와 상용화 시점이 맞물리며 주가가 단기 급등 또는 중장기 상승 트리거가 될 수 있음.
2. 객관적 전망
중장기적으로 주요 임상 이벤트와 기술이전이 주가에 영향을 줄 핵심 변수이며, 상용화 성공 여부가 방향성을 결정할 것.
단, 현재 시총은 기대치를 일부 반영한 상태로, 성과 확인 전까지는 박스권 흐름 또는 이벤트 중심의 단기 변동 가능성 있음.
3. 부정적 전망 (2줄)
주요 임상에서 예상보다 낮은 효능 또는 부작용 리스크가 발생할 경우 기술이전 철회나 주가 급락 가능성 존재.
ADC 경쟁 심화 및 글로벌 시장에서의 후발주자 포지션은 상업화 지연 시 투자 매력도 하락으로 이어질 수 있음.
Disclaimer
- 당사의 모든 콘텐츠는 저작권법의 보호를 받은바, 무단 전재, 복사, 배포 등을 금합니다.
- 콘텐츠에 수록된 내용은 개인적인 견해로서, 당사 및 크리에이터는 그 정확성이나 완전성을 보장할 수 없습니다. 따라서 어떠한 경우에도 본 콘텐츠는 고객의 투자 결과에 대한 법적 책임소재에 대한 증빙 자료로 사용될 수 없습니다.
- 모든 콘텐츠는 외부의 부당한 압력이나 간섭없이 크리에이터의 의견이 반영되었음을 밝힙니다.
